Minerali po njihovom nastanku, sastavu, svojstvima i značenju. Koncept minerala. Hemijski sastav i fizička svojstva minerala. Geologija i njene grane: mineralogija, petrografija, istorijska geologija, tektonika, inženjerska geologija, hidrogeologija
Osnova za klasifikaciju minerala je hemijski sastav minerala. Na osnovu ove karakteristike razlikuju se sljedeće klase minerala: :
Silikati
Hidroksidi (hidroksidi)
Karbonati
Sulfati
Sulfidi
Fosfati
Halogenidi
Izvorni elementi
Organska jedinjenja
Klase minerala i hemijski sastav minerala:
Osnovna karbonatna struktura je jedan atom ugljika vezan za tri atoma kisika. Karbonati uključuju druge elemente kao što su kalcijum, željezo i bakar. Kalcit je najčešći karbonatni mineral. Azurit i malahit, prikazani na donjoj slici, su karbonati koji sadrže bakar umjesto kalcija.
Halogeni minerali su soli koje nastaju kada slana voda isparava. Halit je halogenidni mineral, ali sol nije jedini halogenid. Hemijski elementi poznati kao halogeni vezuju se za različite atome metala i formiraju halogenidne minerale.
Može se izraziti hemijskim formulama - empirijskim i strukturnim. Empirijske formule pokazuju kvantitativni odnos elemenata koji čine mineral. Na primjer, empirijska formula ortoklasa može biti K2 Al2 Si6O16. Ova formula je vrlo pogodna za opisivanje sastava, ali ne odražava prirodu interakcije veza elemenata u strukturi minerala. Ista formula se može dati u obliku molekularnih spojeva različitih oksida, što je pogodno za izražavanje reakcija u kojima učestvuju minerali. Ova formula će se zvati strukturna i može se napisati u ovom obliku: K2 OAl2 O 3 6SiO2
Oksidi sadrže jedan ili dva metalna elementa u kombinaciji s kisikom. Mnogi važni metali javljaju se kao oksidi. Hematit sa dva atoma gvožđa na tri atoma kiseonika i magnetit sa tri atoma gvožđa na četiri atoma kiseonika su oba oksida gvožđa.
Fosfatni minerali su po atomskoj strukturi slični silikatnim mineralima. U fosfatima, fosfor, arsen ili vanadij se vezuju sa kiseonikom i formiraju tetraedre. Postoji mnogo različitih minerala u grupi fosfata, ali većina je rijetka. Sulfatni minerali sadrže atome sumpora vezane za atome kiseonika. Poput halogenida, nastaju tamo gdje isparava slana voda. Grupa sulfata sadrži mnogo različitih minerala, ali samo nekoliko je uobičajenih.
Postoje dvije glavne grupe:
1) Konstantan hemijski sastav (na primer SiO2, FeS2). Ova grupa
minerale je prilično lako proučavati;
2) Minerale koji formiraju direktna jedinjenja prilično je teško proučavati. Ova jedinjenja uključuju minerale koji imaju različite nečistoće (gasovi, rastvori, suspendovane čestice iu obliku pojedinačnih elemenata uključeni u kristalnu rešetku supstance bez narušavanja njenog oblika).
Gips je uobičajeni sulfat s različitim manifestacijama. Pronađeni su ogromni kristali gipsa od 11 metara. To je otprilike isto kao i školski autobus! Iako narandžasti kristali s lijeve strane ne izgledaju kao bijeli pijesak s desne strane, i kristali i pijesak su gipsani.
Sulfidi nastaju kada se metalni elementi spoje sa sumporom. Za razliku od sulfata, sulfidi ne sadrže kiseonik. Pirit, ili željezni sulfid, uobičajen je sulfidni mineral poznat kao zlato budale. Ljudi mogu zamijeniti pirit sa zlatom jer su ta dva minerala sjajna, metalna i žuta.
Mnogi minerali imaju isto hemijski sastav minerala, mogu imati različite strukture i izgled kristali, tekstura, pa samim tim i drugačiji fizička svojstva. Ovo svojstvo minerala naziva se polimorfizam. Primjer polimorfizma je ugljik. U zavisnosti od uslova kristalizacije, može formirati dve poliformne varijante - dijamant i grafit, koji imaju različite rasporede atoma ugljenika u prostoru.
Da bi supstanca bila mineral, mora biti prirodna, neorganska, kristalna solidan, koji ima karakterističan hemijski sastav i kristalnu strukturu. Atomi u mineralima su raspoređeni u pravilne, ponavljajuće obrasce koji se mogu koristiti za identifikaciju tog minerala. Hemijska karakteristika svake grupe: prirodni elementi - samo jedan element; silikati - silika tetraedar; fosfat - fosfatni tetraedar; karbonati - jedan atom ugljika sa tri atoma kiseonika; halogenidi - halogen vezan za atom metala; oksidi - metal u kombinaciji s kisikom; sulfati - sumpor i kiseonik; sulfidi - metal sa sumporom, bez kiseonika. Obsidijan je staklo koje nastaje kada se lava toliko brzo ohladi da atomi nemaju priliku da se rasporede u kristalima. Šta je sa svim mineralima u grupi silikata? Koja je njihova razlika? Jedan uzorak ima hemijski sastav sa omjerom dva atoma željeza prema tri atoma kisika. Drugi uzorak ima hemijski sastav sa omjerom od tri atoma željeza prema četiri atoma kisika. Sadrže iste elemente: jesu li isti mineral? Po čemu se mineralna grupa prirodnih elemenata razlikuje od svih ostalih grupa minerala? Na izletu u Prirodnjački muzej naći ćete dva minerala slične boje. Iz njihovih hemijskih formula jasno je da jedan mineral sadrži elemente cinka, ugljenika i kiseonika. Drugi mineral sadrži elemente cink, silicijum, kiseonik i vodonik. Vaš prijatelj vam kaže da su minerali u istoj grupi minerala. Zašto obsidijan, prirodno staklo koje nastaje hlađenjem lave, a ne mineral? Umjetnici su mljeli mineral azurit kako bi napravili šarene pigmente za boje. Je li azurit u prahu još uvijek kristalan?
- Minerali se dijele u grupe prema svom hemijskom sastavu.
- Šta je kristal?
- Koje elemente sadrže svi silikatni minerali?
- Objasnite svoje rezonovanje.
- Kojih je osam glavnih grupa minerala?
- Zašto se dijamanti ne prave u laboratoriji od minerala?
- Da li je ugalj, nastao prvenstveno od raspadnutih biljaka, mineral?
- Ovo je rok?
Ulazak vode hemijski sastav minerala, dijeli se prema jačini veze: konstitucijski (najčvršće povezan sa kristalnom rešetkom, kristalizacija (također povezan sa kristalnom rešetkom, ali manje čvrsto i stoga se može ukloniti na visokim temperaturama); ziolit (voda, kao da je otopljena u kristalu, dodavanje konstitucijske vode znači stvaranje posebnog oblika minerala, a njegovo uklanjanje uništava mineral.
Kristalna supstanca i njena struktura
Glavna je komponenta raznih vulkanskih stijena kao što su nefelin sijenit, nefelin monzonit i nefelin. Glavna razlika između njih je u različitim omjerima i dostupnim razmacima polja. U nefelinskim monzonitnim stijenama, K-polje i polja plagioklasa su prisutna u približno jednakim omjerima.
Nefelin sadrži samo male dijelove feldspata, a kamen se sastoji pretežno od nefelina. Prirodnog nefelina sa ovom "čistom" hemijom ima vrlo malo, iako čini stabilnu strukturu i namijenjen je upotrebi u proizvodnji keramike i stakla. Ovaj rezultat odražava činjenicu da alkalni položaj natrijuma i kalija ima interesantnu razliku u zahtjevima za prostorom unutar nefelina. Struktura ima.
Dodavanje kristalizacione vode i njeno uklanjanje na visokim temperaturama značajno utiče na mnoga fizička i hemijska svojstva minerala. Na primjer, dodavanjem vode za kristalizaciju, anhidrit se pretvara u gips. Istovremeno, njegov volumen se povećava na 60%. Minerali mogu relativno lako izgubiti i obnoviti ziolitnu vodu, mijenjajući neka njihova svojstva (indeks loma, struktura).
Tu je i četvrti dio, koji je nešto veći od ostala tri. Sa ove veće strane, veći joni kalija bolje odgovaraju. Minerali čija je kemija usko povezana s hemijom alkalnih feldspatova, ali siromašni silikatima, nazivaju se feldspati. Kao rezultat toga, nalaze se u stijenama siromašnim silikatima koje sadrže druge ne-silikatne minerale i kvarc. Da je kvarc bio prisutan tokom procesa kristalizacije, on bi reagovao sa svakim feldspatom i formirao feldspat.
Postoji samo nekoliko nalazišta feldspata. Nefelin reaguje sa kiselinama, ali ne stvara plikove kao mnogi karbonati. Ako se drobi, otapa se u hlorovodoničnoj kiselini i čisti mineralni uzorci bivaju uronjeni u kiselinu, čineći da izgledaju zamućeni ili smrznuti. Ovo može biti korisno u razlikovanju nefelina od sličnih polja, skapolita i kriolita.
Klase minerala - članak na web stranici “student builder.ru”
Minerali su čvrste prirodne formacije koje čine stijene Zemlja, Mjesec i neke druge planete, kao i meteoriti i asteroidi. Minerali su, po pravilu, prilično homogene kristalne supstance uređene unutrašnje strukture i određenog sastava, koji se može izraziti odgovarajućom hemijskom formulom. Minerali nisu mješavina sitnih mineralnih čestica, kao što je šmirgla (sastoji se uglavnom od korunda i magnetita) ili limonita (agregat getita i drugih željeznih hidroksida), već i spojevi elemenata s neuređenom strukturom, poput vulkanskog stakla (opsidijana, itd.) .). Minerali se smatraju hemijskim elementima ili njihovim spojevima nastalim kao rezultat prirodnih procesa. Najvažnije vrste mineralnih sirovina organskog porekla, kao što su ugalj i nafta, isključene su sa liste minerala. Mineralogija je nauka o mineralima, njihovoj klasifikaciji, hemijskom sastavu, karakteristikama i obrascima strukture (strukture), porijeklu, stanju u prirodi i praktična primjena. Za dublje objašnjenje unutrašnja struktura minerala i njihove veze sa istorijom Zemlje, mineralogija uključuje matematiku, fiziku i hemiju. Koristi kvantitativne podatke u većoj mjeri nego druge geološke nauke, jer su za adekvatan opis minerala neophodna fina hemijska analiza i precizna fizička mjerenja.
ISTORIJA MINERALOGIJE
Korištene su kremene ljuspice oštrih rubova primitivni čovek kao oruđe rada već u paleolitu. Kremen (finozrna vrsta kvarca) je dugo bio glavni mineral. Čovjeku su u antičko doba bili poznati i drugi minerali. Neki od njih, kao što su hematit trešnje, žuto-smeđi getit i crni oksidi mangana, korišteni su kao boje za oslikavanje stijena i tijela, dok su drugi, poput ćilibara, žada i samorodnog zlata, korišteni za izradu ritualnih predmeta. , nakit i amajlije. U Egiptu iz preddinastičkog perioda (5000-3000 pne) mnogi minerali su već bili poznati. Za dekoraciju su korišteni samorodni bakar, zlato i srebro. Nešto kasnije, oruđe i oružje počelo se izrađivati od bakra i njegove legure, bronze. Mnogi minerali su korišteni kao boje, drugi za nakit i pečate (tirkiz, žad, kristal, kalcedon, malahit, granat, lapis lazuli i hematit). Trenutno minerali služe kao izvor za proizvodnju metala, građevinskog materijala (cementa, gipsa, stakla, itd.), sirovina za hemijsku industriju, itd. U prvom poznatom spisu o mineralogiji, O kamenju, Aristotelovog učenika, grčki Teofrast (oko 372-287 pne) minerali su bili podijeljeni na metale, zemlju i kamenje. Otprilike 400 godina kasnije, Plinije Stariji (23-79 nove ere), u posljednjih pet knjiga Prirodoslovlja, sažeo je sve informacije o mineralogiji koje su bile dostupne u to vrijeme. IN ranog srednjeg vijeka u zemljama arapskog istoka koje su prihvatile znanje antičke Grčke I drevna Indija, nauka je procvjetala. Centralnoazijski enciklopedist Biruni (973. - oko 1050.) sastavio je opise dragog kamenja (mineralogija) i izumio metodu za precizno mjerenje njihove specifične težine. Još jedan izvanredni naučnik Ibn Sina (Avicena) (oko 980-1037) u svojoj raspravi O kamenju dao je klasifikaciju svih poznatih minerala, dijeleći ih u četiri klase: kamenje i zemlja, fosilna goriva, soli, metali. U srednjem vijeku u Evropi su se prikupljale praktične informacije o mineralima. Rudar i kopač iz nužde su postali mineralozi praktičari i svoje iskustvo i znanje prenosili studentima i šegrtima. Prvi skup činjeničnih informacija o praktičnoj mineralogiji, rudarstvu i metalurgiji bio je rad G. Agricole O metalima (De re metallica), objavljen 1556. Zahvaljujući ovoj raspravi i ranijem djelu O prirodi fosila (De natura fossilium, 1546), koji sadrži klasifikaciju minerala na osnovu njihovih fizičkih svojstava, Agricola je bio poznat kao otac mineralogije. 300 godina nakon objavljivanja Agricolinih radova, istraživanja u oblasti mineralogije bila su posvećena proučavanju prirodnih kristala. 1669. danski prirodnjak N. Stenon, sumirajući svoja zapažanja stotina kristala kvarca, uspostavio je zakon konstantnosti uglova između kristalnih strana. Stoljeće kasnije (1772.) Romé de Lisle je potvrdio Stenonove zaključke. Godine 1784. opat R. Gayuy je postavio temelje modernim idejama o kristalnoj strukturi. Godine 1809. Wollaston je izumio reflektivni goniometar, koji je omogućio preciznija mjerenja uglova između strana kristala, a 1812. iznio je koncept prostorne rešetke kao zakona unutrašnje strukture kristala. 1815. P. Cordier je predložio studiranje optička svojstva fragmenti usitnjenih minerala pod mikroskopom. Dalji razvoj mikroskopskih istraživanja povezan je sa pronalaskom W. Nicola 1828. uređaja za proizvodnju polarizirane svjetlosti (Nicol prizma). Polarizacioni mikroskop je 1849. poboljšao G. Sorby, koji ga je primenio na proučavanje providnih tankih preseka stena. Postojala je potreba za klasifikacijom minerala. C. Linnaeus je 1735. godine objavio djelo Sistem prirode (Systema naturae), u kojem su minerali razvrstani prema vanjskim karakteristikama, tj. baš kao i biljke i životinje. Zatim su švedski naučnici - A. Kronstedt 1757. i J. Berzelius 1815. i 1824. - predložili nekoliko opcija hemijske klasifikacije minerali. Druga Berzeliusova klasifikacija, koju je modificirao K. Rammelsberg 1841.-1847., čvrsto je uspostavljena nakon što ju je američki mineralog J. Dana upotrijebio kao osnovu za treće izdanje Dana's System of Mineralogy, 1850. Veliki doprinos razvoju mineralogije u 18 - u prvoj polovini 19. veka, nemački naučnici A.G.Werner i I.A.Breithaupt i Rusi - M.V.Lomonosov i V.M.Severgin uveli su poboljšane polarizacione mikroskope, optičke goniometre i analitičke metode Kada su kristali počeli da se proučavaju pomoću rendgenske analize, došlo je do dubljeg razumevanja strukture minerala. preko njih Ova metoda je revolucionirala mineralogiju: pretežno deskriptivna nauka postala je preciznija i mineralozi su mogli povezati fizička i hemijska svojstva minerala sa njihovim kristalnim strukturama. Krajem 19. - početkom 20. vijeka. Razvoj mineralogije bio je uveliko olakšan radom istaknutih ruskih naučnika, V.I.Fedorova, A.K. mineralogija je usvojila nove istraživačke metode fizike čvrstog stanja, posebno infracrvenu spektroskopiju, čitav niz rezonantnih metoda (elektronska paramagnetna rezonanca, nuklearna gama rezonancija itd.), luminescentnu spektroskopiju itd., kao i najnovije analitičke metode, uključujući analizu elektronskom mikrosondom, elektronsku mikroskopiju u kombinaciji sa difrakcijom elektrona, itd. Upotreba ovih metoda omogućava određivanje hemijskog sastava minerala „u tački“, tj. na pojedinim zrncima minerala, proučavati suptilne karakteristike njihove kristalne strukture, sadržaj i distribuciju elemenata nečistoća, prirodu boje i luminescencije. Uvođenje preciznih fizičkih istraživačkih metoda proizvelo je pravu revoluciju u mineralogiji. Imena takvih ruskih naučnika kao što su N.V. Belov, D.S. Koržinski, D.P. Grigoriev, I.I.
GLAVNA SVOJSTVA MINERALA
Dugo vremena glavne karakteristike minerala bile su spoljašnji oblik njihovi kristali i drugi sekreti, kao i fizička svojstva (boja, sjaj, cijepanje, tvrdoća, gustina itd.), koja i danas postoje veliki značaj u njihovom opisu i vizuelnoj (posebno terenskoj) dijagnostici. Ove karakteristike, kao i optička, hemijska, električna, magnetna i druga svojstva, zavise od hemijskog sastava i unutrašnje strukture (kristalne strukture) minerala. Primarna uloga hemije u mineralogiji prepoznata je sredinom 19. stoljeća, ali je važnost strukture postala očigledna tek uvođenjem radiografije. Prvo dekodiranje kristalnih struktura izveli su već 1913. godine engleski fizičari W. G. Bragg i W. L. Bragg. Minerali su hemijska jedinjenja (sa izuzetkom prirodnih elemenata). Međutim, čak i bezbojni, optički prozirni uzorci ovih minerala gotovo uvijek sadrže male količine nečistoća. Prirodne otopine ili taline iz kojih kristaliziraju minerali obično se sastoje od mnogo elemenata. Tokom formiranja spojeva, nekoliko atoma manje uobičajenih elemenata može zamijeniti atome glavnih elemenata. Takva supstitucija je toliko uobičajena da se hemijski sastav mnogih minerala vrlo rijetko približava sastavu čistog spoja. Na primjer, sastav običnog kamenotvornog minerala olivina varira unutar sastava dva tzv. krajnji članovi serije: od forsterita, magnezijum silikata Mg2SiO4, do fajalita, željeznog silikata Fe2SiO4. Odnos Mg:Si:O u prvom mineralu i Fe:Si:O u drugom je 2:1:4. Kod olivina srednjeg sastava omjeri su isti, tj. (Mg + Fe):Si:O je 2:1:4, a formula je napisana kao (Mg,Fe)2SiO4. Ako su poznate relativne količine magnezijuma i gvožđa, onda se to može odraziti na formulu (Mg0,80Fe0,20)2SiO4, iz koje se vidi da je 80% atoma metala predstavljeno magnezijumom, a 20% gvožđe.
Struktura. Svi minerali, sa izuzetkom vode (koja se – za razliku od leda – obično ne klasifikuje kao minerali) i žive, su čvrste materije na uobičajenim temperaturama. Međutim, ako se voda i živa jako ohlade, oni se stvrdnjavaju: voda na 0°C, a živa na -39°C. Na ovim temperaturama, molekule vode i atomi žive formiraju karakterističnu pravilnu trodimenzionalnu kristalnu strukturu (izrazi "kristalni " i "čvrsto") " u ovom slučaju su gotovo ekvivalentni). Dakle, minerali su kristalne tvari čija su svojstva određena geometrijskim rasporedom njihovih sastavnih atoma i vrstom kemijske veze između njih. Jedinična ćelija (najmanja podjela kristala) sastoji se od pravilno raspoređenih atoma koji se drže zajedno elektronskim vezama. Ove sićušne ćelije, koje se beskonačno ponavljaju u trodimenzionalnom prostoru, formiraju kristal. Veličine jediničnih ćelija u različitim mineralima su različite i zavise od veličine, broja i relativnog rasporeda atoma unutar ćelije. Parametri ćelije su izraženi u angstromima () ili nanometrima (1 = 10-8 cm = 0,1 nm). Elementarne ćelije kristala spojene čvrsto, bez praznina, ispunjavaju volumen i formiraju kristalnu rešetku. Kristali se dijele na osnovu simetrije jedinične ćelije, koju karakterizira odnos između njenih rubova i uglova. Obično postoji 7 sistema (po redoslijedu povećanja simetrije): triklinički, monoklinski, rombični, tetragonalni, trigonalni, heksagonalni i kubni (izometrijski). Ponekad trigonalni i heksagonalni sistemi nisu razdvojeni i opisuju se zajedno pod nazivom heksagonalni sistem. Singonije su podijeljene u 32 kristalne klase (vrste simetrije), uključujući 230 prostornih grupa. Ove grupe je prvi put identifikovao ruski naučnik E.S. Fedorov 1890. Analizom rendgenske difrakcije određuju se dimenzije jedinične ćelije minerala, njegova singonija, klasa simetrije i prostorna grupa, te se dešifruje kristalna struktura, tj. relativni položaj atoma koji čine jediničnu ćeliju u trodimenzionalnom prostoru.
GEOMETRIJSKA (MORFOLOŠKA) KRISTALOGRAFIJA
Kristali sa svojim ravnim, glatkim, sjajnim ivicama dugo su privlačili ljudsku pažnju. Od pojave mineralogije kao nauke, kristalografija je postala osnova za proučavanje morfologije i strukture minerala. Utvrđeno je da lica kristala imaju simetričan raspored, što omogućava da se kristal pripiše određenom sistemu, a ponekad i jednoj od klasa (simetrija) (vidi gore). Rentgenske studije su pokazale da vanjska simetrija kristala odgovara unutrašnjem pravilnom rasporedu atoma. Veličine mineralnih kristala variraju u vrlo širokom rasponu - od divova teških 5 tona (masa dobro oblikovanog kvarcnog kristala iz Brazila) do tako malih da se njihova lica mogu razlikovati samo pod elektronskim mikroskopom. Kristalni oblik čak i istog minerala može se neznatno razlikovati u različitim uzorcima; na primjer, kristali kvarca su gotovo izometrijski, iglasti ili spljošteni. Međutim, svi kristali kvarca, veliki i mali, šiljasti i ravni, nastaju ponavljanjem identičnih jediničnih ćelija. Ako su ove ćelije orijentirane u određenom smjeru, kristal ima izdužen oblik, a ako je u dva smjera na štetu trećeg, tada je oblik kristala tabelarni. Budući da uglovi između odgovarajućih strana istog kristala imaju konstantnu vrijednost i specifični su za svaku vrstu minerala, ova karakteristika je nužno uključena u karakteristike minerala. Minerali predstavljeni pojedinačnim dobro rezanim kristalima su rijetki. Mnogo češće se javljaju u obliku nepravilnih zrnaca ili kristalnih agregata. Često mineral karakterizira određena vrsta agregata, koji može poslužiti kao dijagnostičko svojstvo. Postoji nekoliko tipova jedinica. Dendritski razgranati agregati podsjećaju na lišće paprati ili mahovinu i karakteristični su, na primjer, za piroluzit. Vlaknasti agregati koji se sastoje od gusto zbijenih paralelnih vlakana tipični su za krizotil i amfibol azbest. Kolomorfni agregati, koji imaju glatku, zaobljenu površinu, izgrađeni su od vlakana koja se protežu radijalno od zajedničkog centra. Velike okrugle mase su mastoidne (malahit), dok su manje bubrežaste (hematit) ili grožđaste (psilomelan).
Ljuskasti agregati koji se sastoje od malih pločastih kristala karakteristični su za liskun i barit. Stalaktiti su nakapane formacije koje vise u obliku ledenica, cijevi, čunjeva ili „zavjesa“ u kraškim pećinama. Nastaju kao rezultat isparavanja mineralizirane vode koja prodire kroz krečnjačke pukotine, a često se sastoje od kalcita (kalcij karbonata) ili aragonita. Ooliti, agregati koji se sastoje od malih kuglica i nalik na riblja jaja, nalaze se u nekim kalcitima (oolitni krečnjak), getitom (oolitna željezna ruda) i drugim sličnim formacijama.
CRYSTAL CHEMISTRY
Nakon akumulacije rendgenskih podataka i poređenja sa rezultatima hemijskih analiza, postalo je očigledno da karakteristike kristalne strukture minerala zavise od njegovog hemijskog sastava. Tako su postavljeni temelji nova nauka - kristalna hemija. Mnoga naizgled nepovezana svojstva minerala mogu se objasniti uzimajući u obzir njihovu kristalnu strukturu i hemijski sastav. Neki hemijski elementi (zlato, srebro, bakar) nalaze se u nativnim, tj. čista, forma. Građeni su od električno neutralnih atoma (za razliku od većine minerala, čiji atomi nose električni naboj i nazivaju se joni). Atom s nedostatkom elektrona je pozitivno nabijen i naziva se kation; atom s viškom elektrona ima negativan naboj i naziva se anion. Privlačenje između suprotno nabijenih jona naziva se ionsko vezanje i služi kao glavna sila vezivanja u mineralima. S drugom vrstom veze, vanjski elektroni rotiraju oko jezgara u zajedničkim orbitama, povezujući atome jedan s drugim. Kovalentna veza je najjača vrsta veze. Minerali s kovalentnim vezama obično imaju visoku tvrdoću i tačku (na primjer, dijamant). Mnogo manju ulogu u mineralima igra slaba van der Waalsova veza koja se javlja između električno neutralnih strukturnih jedinica. Energija vezivanja takvih strukturnih jedinica (slojeva ili grupa atoma) je neravnomjerno raspoređena. Van der Waalsove veze pružaju privlačnost između suprotno nabijenih regija u većim strukturnim jedinicama. Ova vrsta veze se uočava između slojeva grafita (jedan od prirodnih oblika ugljika), nastalih zbog jake kovalentne veze atoma ugljika. Zbog slabe veze između slojeva, grafit ima malu tvrdoću i vrlo savršeno cijepanje, paralelno sa slojevima. Stoga se grafit koristi kao mazivo. Suprotno nabijeni ioni približavaju se jedni drugima do udaljenosti na kojoj odbojna sila uravnotežuje privlačnu silu. Za bilo koji određeni par katjon-anion, ova kritična udaljenost je jednaka zbiru "radijusa" dva jona. Određivanjem kritičnih udaljenosti između različitih jona, bilo je moguće odrediti veličinu radijusa većine jona (u nanometrima, nm). Budući da većinu minerala karakteriziraju jonske veze, njihove strukture se mogu vizualizirati u obliku kuglica koje se dodiruju. Strukture ionskih kristala uglavnom zavise od veličine i znaka naboja i relativne veličine jona. Pošto je kristal u cjelini električno neutralan, zbir pozitivnih naboja jona mora biti jednak zbiru negativnih. U natrijum hloridu (NaCl, mineral halit) svaki natrijum jon ima naelektrisanje od +1, a svaki hloridni jon -1 (slika 1), tj. Svaki ion natrijuma odgovara jednom jonu hlora. Međutim, u fluoritu (kalcijum fluorid, CaF2), svaki kalcijum ion ima naelektrisanje od +2, a svaki fluoridni ion ima naelektrisanje od -1. Stoga, da bi se održala ukupna električna neutralnost jona fluora, ona mora biti dvostruko veća od jona kalcijuma (slika 2).
Karakterističan je i sjaj nefelina poput masti. Masivni nefelin ima masni sjaj i nazvan je Eleolit. Ovo ime dolazi iz grčkog i znači Tsl. Nefelin je takođe pozajmljen iz grčki jezik i znači oblak kao aluziju na mutne ili prozirne kristale i mase.
Dakle, izraz "pijesak" odnosi se na određeni raspon veličine zrna. Za razliku od većine drugih stijena, pješčenjak nije definiran specifičnom mineralnom populacijom. Glavni mineral se obično smatra kvarc. Pojedinačna zrna pijeska, komponente, također mogu biti sastavljena od drugih minerala ili fragmenata stijena. Pješčanik čije se komponente sastoje od više od 90% kvarcnih zrna naziva se kvarcni pješčenjak.
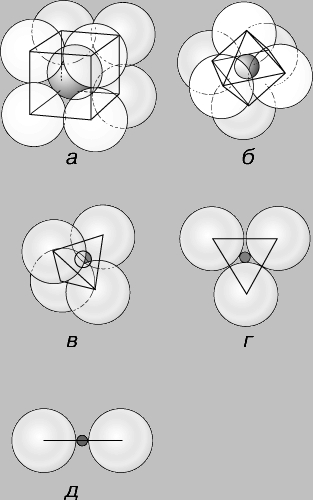
Mogućnost njihovog uključivanja u datu kristalnu strukturu zavisi i od veličine jona. Ako su joni iste veličine i spakovani na takav način da svaki ion dodiruje 12 drugih, onda su u odgovarajućoj koordinaciji. Postoje dva načina pakovanja sfera iste veličine (slika 3): kubično blisko pakovanje, koje generalno dovodi do formiranja izometrijskih kristala, i heksagonalno blisko pakovanje, koje formira heksagonalne kristale. U pravilu, kationi su manje veličine od aniona, a njihove veličine su izražene u dijelovima radijusa aniona, uzetim kao jedan. Obično se koristi omjer dobiven dijeljenjem radijusa kationa sa radijusom anjona. Ako je kation samo malo manji od aniona s kojima se kombinuje, može biti u kontaktu sa osam aniona koji ga okružuju, ili, kako se obično kaže, u osmostrukoj koordinaciji u odnosu na anione koji se nalaze, takoreći, na vrhovima kocke oko njega. Ova koordinacija (koja se naziva i kubična) je stabilna pri omjerima jonskog radijusa od 1 do 0,732 (slika 4a). Pri manjem omjeru jonskog radijusa, osam anjona se ne može složiti da bi dodirnuli kation. U takvim slučajevima, geometrija pakovanja omogućava šestostruku koordinaciju kationa sa anjonima koji se nalaze na šest vrhova oktaedra (slika 4b), koji će biti stabilni pri odnosima njihovih poluprečnika od 0,732 do 0,416. Daljnjim smanjenjem relativne veličine kationa dolazi do prijelaza na četverostruku ili tetraedarsku koordinaciju, stabilnu pri omjerima radijusa od 0,414 do 0,225 (slika 4c), zatim na trostruku koordinaciju unutar omjera radijusa od 0,225 do 0,155 (sl. 4c d) i dvostruki - sa omjerom radijusa manjim od 0,155 (slika 4,e). Iako drugi faktori takođe određuju tip koordinacionog poliedra, za većinu minerala princip odnosa jonskog radijusa je jedno efikasno sredstvo za predviđanje kristalne strukture.

Posebno označeni peščari
Odnosi se na stijenu glavnih agregata kalcita i kvarca. Odnosi se na poligensku stijenu pretežno tamno sivo-smeđe-sive boje sa kotlovima od kvarca, silicijumskog škriljevca, feldspata, ali posebno mljevenih škriljaca. Oni su pokazatelj niskog nivoa transporta u obrazovanju. Pješčari su sedimentne ili sedimentne stijene nastale od rastresitog pijeska, sedimenta, stvrdnjavanjem. Vozila su voda, vjetar i led. Do taloženja pijeska dolazi zbog gravitacije kroz mehanički paragraf.
Minerali potpuno različitog kemijskog sastava mogu imati slične strukture koje se mogu opisati korištenjem istih koordinacijskih poliedra. Na primjer, u natrijum hloridu NaCl, odnos radijusa natrijum jona i poluprečnika jona hlora je 0,535, što ukazuje na oktaedarsku ili šesterostruku koordinaciju. Ako se oko svakog kationa grupiše šest anjona, onda da bi se održao odnos kationa i anjona 1:1, oko svakog anjona mora biti šest kationa. Ovo proizvodi kubičnu strukturu poznatu kao struktura tipa natrijum hlorida. Iako se ionski radijusi olova i sumpora oštro razlikuju od ionskih radijusa natrijuma i hlora, njihov omjer također određuje šesterostruku koordinaciju, stoga PbS galena ima strukturu tipa natrijevog klorida, tj. halit i galena su izostrukturni. Nečistoće u mineralima obično su prisutne u obliku jona koji zamjenjuju one minerala domaćina. Takve zamjene uvelike utiču na veličinu iona. Ako su radijusi dva jona jednaki ili se razlikuju za manje od 15%, oni se lako zamjenjuju. Ako je ova razlika 15-30%, takva zamjena je ograničena; sa razlikom većom od 30%, zamjena je praktično nemoguća. Postoji mnogo primjera parova izostrukturnih minerala sa sličnim kemijskim sastavom između kojih dolazi do ionske supstitucije. Dakle, karbonati siderit (FeCO3) i rodohrozit (MnCO3) imaju sličnu strukturu, a željezo i mangan se mogu zamijeniti u bilo kojem odnosu, formirajući tzv. čvrstih rastvora. Između ova dva minerala postoji neprekidan niz čvrstih rastvora. U drugim parovima minerala, joni imaju ograničene mogućnosti za međusobnu supstituciju. Pošto su minerali električno neutralni, naboj jona utiče i na njihovu međusobnu supstituciju. Ako se supstitucija dogodi sa suprotno nabijenim jonom, tada se u nekom dijelu ove strukture mora dogoditi druga supstitucija, u kojoj naboj zamjenskog jona kompenzira narušavanje električne neutralnosti uzrokovano prvim. Ova konjugirana supstitucija je zabilježena u feldspars- plagioklase, kada kalcij (Ca2+) zamjenjuje natrijum (Na+) formiranjem kontinuiranog niza čvrstih otopina. Višak pozitivnog naboja koji nastaje zamjenom Na+ jona ionom Ca2+ kompenzira se istovremenom zamjenom silicijuma (Si4+) s aluminijem (Al3+) u susjednim dijelovima strukture.
FIZIČKA SVOJSTVA MINERALA
Iako se glavne karakteristike minerala (hemijski sastav i unutrašnja kristalna struktura) utvrđuju na osnovu hemijskih analiza i rendgenske difrakcije, one se indirektno odražavaju na svojstva koja se lako uočavaju ili mere. Za dijagnosticiranje većine minerala dovoljno je odrediti njihov sjaj, boju, cijepanje, tvrdoću i gustoću. Sjaj je kvalitativna karakteristika svjetlosti koju reflektuje mineral. Neki neprozirni minerali snažno reflektiraju svjetlost i imaju metalni sjaj. Ovo je uobičajeno u rudnim mineralima kao što su galena (minerali olova), halkopirit i bornit (minerali bakra), argentit i akantit (minerali srebra). Većina minerala apsorbira ili prenosi značajan dio svjetlosti koja pada na njih i imaju nemetalni sjaj. Neki minerali imaju sjaj koji prelazi iz metalnog u nemetalni, što se naziva polumetalnim. Minerali s nemetalnim sjajem obično su svijetle boje, neki od njih su prozirni. Kvarc, gips i lagani liskun su često prozirni. Ostali minerali (na primjer, mliječno bijeli kvarc) koji prenose svjetlost, ali kroz koje se objekti ne mogu jasno razlikovati, nazivaju se prozirnim. Minerali koji sadrže metale razlikuju se od ostalih po propuštanju svjetlosti. Ako svjetlost prolazi kroz mineral, barem u najtanjim rubovima zrna, onda je on, po pravilu, nemetalni; ako svjetlost ne prolazi, onda je to ruda. Postoje, međutim, izuzeci: na primjer, sfalerit svijetle boje (mineral cinka) ili cinabar (mineral žive) često su prozirni ili prozirni. Minerali se razlikuju po kvalitativnim karakteristikama svog nemetalnog sjaja. Glina ima dosadan, zemljani sjaj. Kvarc na rubovima kristala ili na lomnim površinama je staklast, talk, koji je podijeljen na tanke listove duž ravnina cijepanja, je sedef. Svijetli, svjetlucavi, poput dijamanta, sjaj se naziva dijamant. Kada svjetlost padne na mineral nemetalnog sjaja, djelomično se odbija od površine minerala, a djelomično se lomi na ovoj granici. Svaku tvar karakterizira određeni indeks loma. Budući da se može mjeriti s velikom preciznošću, to je vrlo korisna mineralna dijagnostička karakteristika. Priroda sjaja zavisi od indeksa prelamanja, a oba zavise od hemijskog sastava i kristalne strukture minerala. Općenito, transparentni minerali koji sadrže atome teških metala odlikuju se visokim sjajem i visokim indeksom prelamanja. Ova grupa uključuje uobičajene minerale kao što su anglezit (olovni sulfat), kasiterit (kositrov oksid) i titanit ili sfen (kalcijum titan silikat). Minerali sastavljeni od relativno lakih elemenata takođe mogu imati visok sjaj i visok indeks prelamanja ako su njihovi atomi čvrsto zbijeni i drže zajedno jakim hemijskim vezama. Upečatljiv primjer je dijamant, koji se sastoji od samo jednog svjetlosnog elementa, ugljika. U manjoj mjeri to vrijedi i za mineral korund (Al2O3), čije su prozirne boje - rubin i safir. drago kamenje. Iako se korund sastoji od lakih atoma aluminija i kisika, oni su tako čvrsto povezani da mineral ima prilično jak sjaj i relativno visok indeks loma. Neka sjajila (masna, voštana, mat, svilenkasta, itd.) ovise o stanju površine minerala ili o strukturi mineralnog agregata; smolasti sjaj karakterističan je za mnoge amorfne supstance (uključujući minerale koji sadrže radioaktivne elemente uranijum ili torijum). Boja je jednostavan i praktičan dijagnostički znak. Primjeri uključuju mesingano-žuti pirit (FeS2), olovno-sivi galenit (PbS) i srebrno-bijeli arsenopirit (FeAsS2). Kod drugih rudnih minerala metalnog ili polumetalnog sjaja, karakteristična boja može biti maskirana igrom svjetlosti u tankom površinskom filmu (tamnjenje). Ovo je uobičajeno za većinu minerala bakra, posebno bornita, koji se naziva "paunova ruda" zbog svoje prelive plavo-zelene mrlje koja se brzo razvija kada se svježe lomi. Međutim, drugi minerali bakra obojeni su poznatim bojama: malahit - zelena, azurit - plava. Neki nemetalni minerali su nepogrešivo prepoznatljivi po boji određenoj glavnim hemijskim elementom (žuta - sumpor i crna - tamno siva - grafit itd.). Mnogi nemetalni minerali sastoje se od elemenata koji im ne daju određenu boju, ali imaju obojene varijante, čija je boja posljedica prisustva nečistoća kemijskih elemenata u malim količinama koje nisu uporedive sa intenzitetom boju koju uzrokuju. Takvi elementi se nazivaju hromofori; njihove jone karakterizira selektivna apsorpcija svjetlosti. Na primjer, tamno ljubičasti ametist duguje svoju boju beznačajnoj primjesi željeza u kvarcu i debelom zelene boje smaragd je povezan sa malim sadržajem hroma u berilu. Boje u normalno bezbojnim mineralima mogu biti rezultat defekata u kristalnoj strukturi (uzrokovanih nepopunjenim atomskim pozicijama u rešetki ili ugradnjom stranih jona), što može uzrokovati selektivnu apsorpciju određenih valnih dužina u spektru bijele svjetlosti. Zatim se minerali farbaju u dodatne boje. Rubini, safiri i aleksandriti duguju svoju boju upravo ovim svjetlosnim efektima. Bezbojni minerali mogu biti obojeni mehaničkim inkluzijama. Tako tanko raspršeno širenje hematita daje kvarcu crvenu boju, kloritu - zelenu. Mliječni kvarc je zamućen gasno-tečnim inkluzijama. Iako je mineralna boja jedno od najlakše odredivih svojstava u mineralnoj dijagnostici, mora se koristiti s oprezom jer ovisi o mnogim faktorima. Uprkos varijabilnosti boje mnogih minerala, boja mineralnog praha je vrlo stalna, te je stoga važna dijagnostička karakteristika. Obično je boja mineralnog praha određena linijom (tzv. „boja linije“) koju mineral ostavlja kada se pređe preko neglaziranog porculanskog tanjira (keksa). Na primjer, mineral fluorit je obojen različite boje, ali njegova linija je uvijek bela.
Cleavage. Karakteristično svojstvo minerala je njihovo ponašanje pri cijepanju. Na primjer, kvarc i turmalin, čija površina loma podsjeća na staklenu strugotinu, imaju konhoidnu frakturu. Kod drugih minerala, lom se može opisati kao hrapav, nazubljen ili razbijen. Za mnoge minerale karakteristika nije lom, već cijepanje. To znači da se cijepaju duž glatkih ravni koje su direktno povezane s njihovom kristalnom strukturom. Sile vezivanja između ravnina kristalne rešetke mogu varirati ovisno o kristalografskom smjeru. Ako su u nekim smjerovima mnogo veći nego u drugim, tada će se mineral podijeliti preko najslabije veze. Pošto je cijepanje uvijek paralelno s atomskim ravnima, može se označiti navođenjem kristalografskih smjerova. Na primjer, halit (NaCl) ima kockasti cijepanje, tj. tri međusobno okomita pravca mogućeg razdvajanja. Rascjep također karakterizira lakoća ispoljavanja i kvalitet rezultirajuće površine cijepanja. Liskun ima veoma savršen dekolte u jednom pravcu, tj. lako se cijepa na vrlo tanke listove sa glatkom sjajnom površinom. Topaz ima savršeno cijepanje u jednom smjeru. Minerali mogu imati dva, tri, četiri ili šest smjerova cijepanja duž kojih ih je podjednako lako cijepati, ili nekoliko smjerova cijepanja različitog stepena. Neki minerali se uopće ne cijepaju. Kako je cijepanje, kao manifestacija unutrašnje strukture minerala, njihovo stalno svojstvo, ono služi kao važno dijagnostičko svojstvo. Tvrdoća je otpornost koju mineral pokazuje kada se ogrebe. Tvrdoća ovisi o kristalnoj strukturi: što su atomi u strukturi minerala čvršće povezani, to je teže ogrebati. Talk i grafit su mekani minerali nalik pločama, izgrađeni od slojeva atoma povezanih vrlo slabim silama. Masni su na dodir: kada se trljaju o kožu ruku, pojedinačni tanki slojevi skliznu. Većina tvrdi mineral- dijamant u kojem su atomi ugljika tako čvrsto povezani da ga može izgrebati samo drugi dijamant. Početkom 19. vijeka. Austrijski mineralog F. Moos rasporedio je 10 minerala po rastućem redoslijedu njihove tvrdoće. Od tada se koriste kao standardi za relativnu tvrdoću minerala, tzv. Mohsova skala (tabela 1). Tabela 1.
MOH SKALA TVRDOĆE
